- Con questo esperimento replicheremo il progetto dello scienziato Alessandro Volta che nel 1799 elaborò una pila, attraverso la quale per un processo di ossiduriduzione si trasforma energia chimica in energia elettrica
Attrezzature necessarie
Per effettuare l’esperimento sono necessarie le seguenti attrezzature (figura 1):
- Carta stagnola
- Dei centesimi
- Dello scottex
- Del sale
- Un contenitore con acqua (non in foto)
- Un paio di forbici
- Un voltmetro o un led o un qualsiasi apparecchio elettrico a bassa tensione
 |
| Figura 1 |
Spiegazione della teoria necessaria per l’esperimento
Una pila è uno strumento che consente la conversione di energia chimica ad energia elettrica per mezzo di una reazione di ossidoriduzione. Una pila è composta dai seguenti elementi:
- Due elettrodi che sono i poli della pila
- Una soluzione elettrolitica (polare), che permette il passaggio degli ioni
- Un filo di materiale conduttore
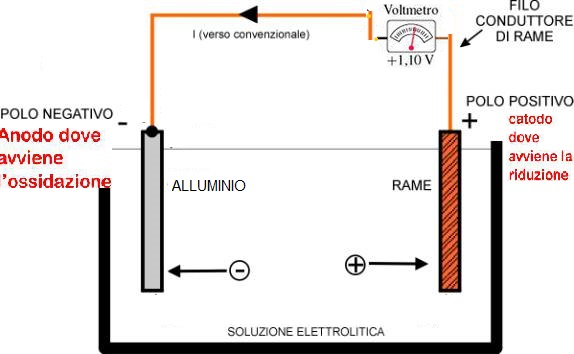 |
| Schema pila |
 |
SCALA DEI POTENZIALI DI OSSIDAZIONE |
 |
SCALA DEI POTENZIALI DI RIDUZIONE |
Qualsiasi coppia di metalli se messi in contatto hanno una tendenza a ossidarsi o ridursi nel nostro caso
al catodo avviene la reazione di riduzione:
Cu2+(aq) + 2 e− → Cu(s)
(Eº = +0,34 V) potenziale di riduzione, la sua tendenza a ridursi
All’anodo avviene la reazione di ossidazione:
Al(s) → Al3+(aq) + 3 e−
(Eº = −1,67)
Si crea quindi una differenza di potenziale fra i due elettrodi e ció porta a un passaggio di corrente.
COME SVOLGERE L’ESPERIMENTO
- Per prima cosa realizziamo dei dischi di scottex e di carta stagnola grandi come le monete (un consiglio é piegare la carta prima di tagliarla)
- Successivamente occorre mettere un foglio di alluminio con sopra un tondino di scottex imbevuto in acqua e sale che funge da soluzione elettrolita e una monetina (questo insieme di cose forma l’elemento della pila, la tensione per ogni elemento della pila é 0,7 V circa
- Ora misuriamo l’elemento con il tester

- Per avere un voltaggio maggiore ci basta semplicemente mettere piú elementi in serie ovvero mettere a contatto l’alluminio di un elemento con la moneta dell’altro (il voltaggio finale sará la somma dei volt di ogni elemento) e se vogliamo possiamo anche mettere in serie delle comuni pile stilo.
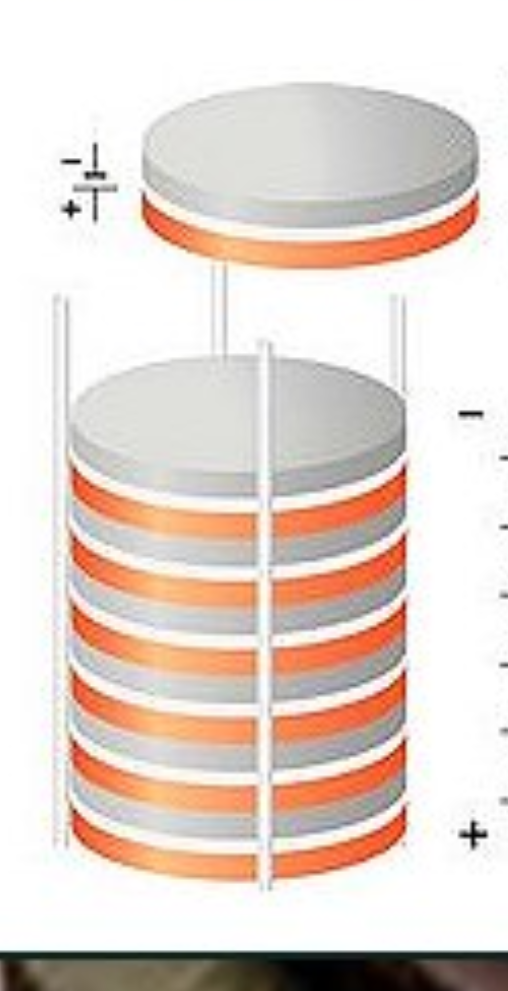
- Schema di una serie (sopra)

- Ora possiamo provare a alimentare qualcosa con le nostre pile!
- Ad esempio un laser

 Se andiamo a controllare le nostre pile dopo un po di tempo questo é quello che vedremo.
Se andiamo a controllare le nostre pile dopo un po di tempo questo é quello che vedremo. 
Le monete sono come incrostate dalla parte che é a contatto con lo scottex ció avviene perché per la reazione di riduzione di prima gli ioni si depositano sul catodo e lo fanno ingrossare.
Articolo redatto dall’alunno Cavagnetto Marco della classe IV A sotto la supervisione dell’ illuminato prof. Paolo Baracani e del nonno, esperto perito elettrotecnico, Marcello Fiori.


Commenti recenti